朱棣,中科院上海生化細胞所博士畢業(yè),哈佛大學博士后,現(xiàn)任復旦大學藥學院研究員、博士研究生導師;上海浦東復旦大學張江科技研究院研究員;2016年入選國家青年“*人計劃”,2015年受聘為哈佛大學醫(yī)學院醫(yī)學講師(Instructor/faculty)。現(xiàn)任中國藥理學學會化藥專業(yè)委員會委員、中國博士后科學基金會評委、中國老年學和老年醫(yī)學學會腫瘤分會專家委員會專委、美國AACR和ASCO會員。
主要研究領域、方向:1.腫瘤免疫藥理學機制研究;2.腫瘤靶向治療新藥開發(fā)。
致力于轉化醫(yī)學和藥物早期發(fā)現(xiàn)的研究,在靶點驗證和新藥早期研發(fā)領域中積累多年經驗。完成了第一個癌癥特異性的多肽類Wnt信號通路抑制劑的研究和發(fā)現(xiàn),開發(fā)出了針對BCL9/β-catenin的First-in-class抑制劑;建立了第一個以骨髓內皮細胞為基質的骨髓轉移體內動物模型的建立,發(fā)現(xiàn)了CyPA-CD147信號通路介導的骨髓微環(huán)境的腫瘤細胞轉移的機制研究,提供了一種多發(fā)性骨髓瘤潛在的新的治療靶點,填補了多發(fā)性骨髓瘤中轉移機制研究空白,鑒定出了新的潛在的診斷靶點Cyclophilin A,為臨床階段新藥CD147單抗提供了在多發(fā)性骨髓瘤中的潛在的新的適應癥,為多發(fā)性骨髓瘤提供了潛在的新的治療方法。
教育經歷
2001.09—2005.07 山東大學生物化學與分子生物學專業(yè)本科生
2005.09—2010.07 中國科學院研究生院生物化學與分子生物學專業(yè)博士研究生
工作經歷
2011.01—2015.06 美國哈佛大學Dana-Farber 癌癥研究所博士后
2015.07—2016.05 美國哈佛大學Dana-Farber 癌癥研究所講師(junior faculty)
2016.10— 2021.07 復旦大學藥學院,博士生導師
2017.01— 至今 復旦大學附屬閔行醫(yī)院兼職教授
2021.08— 至今 復旦大學基礎醫(yī)學院,博士生導師
學術兼職
2017-今 中國藥理學會 會員
2018-今 上海市藥理學會 會員
2019-今 中國老年學和老年醫(yī)學學會老年腫瘤分會專家委員會 專業(yè)委員
2021-今 中國藥理學會化藥專業(yè)委員會 專業(yè)委員
2022-今 中國抗癌協(xié)會 會員
主講課程:
本科生課程:
藥理學、口腔臨床藥物學、藥學分子生物學、生物化學
研究生課程:
高級藥理學進展、高級臨床藥理學、高級神經藥理學、藥學進展
博士后招聘:
復旦大學基礎醫(yī)學院藥理學系朱棣組招聘博士后
復旦大學基礎醫(yī)學院藥理系朱棣組現(xiàn)面向國內外招聘具有腫瘤藥理學、 腫瘤細胞生物學、免疫學背景的博士后。
實驗室主要針對腫瘤免疫微環(huán)境的Wnt信號通路,從分子水平、細胞水平、動物模型及臨床樣本上系統(tǒng)地研究腫瘤免疫反應中的信號作用機制,方向主要為轉化醫(yī)學和早期藥物發(fā)現(xiàn)的研究,更側重于利用單細胞測序技術研究腫瘤微環(huán)境中免疫細胞,腫瘤細胞作用的主要機制,以及新靶標藥物篩選和其作用機制研究,期望鑒定出可用于藥物篩選的分子靶標或可用于臨床的先導化合物,并提出免疫診斷及治療的新途徑。
課題組長朱棣教授主要從事腫瘤免疫藥理學機制以及腫瘤靶向治療新藥開發(fā)分子機制研究,現(xiàn)為復旦大學基礎醫(yī)學院博士生導師,復旦大學附屬閔行醫(yī)院兼職教授。其研究成果以第一或通訊作者發(fā)表在Nature Medicine,Cancer Discovery, Signal Transduction and Targeted Therapy, Science Translational Medicine , Science Advances, Oncogene,British Journal of Pharmacology,Pharmacological Research等雜志,總共發(fā)表SCI論文24篇,單篇最高影響因子53。 并獲得“國家青年特聘專家”、“ 復旦卓識人才”等稱號。主持項目11項,參與4項。申請國際專利4項,授權2項;國內專利6項。2項科研成果已經進入非注冊臨床試驗。受邀在2017年美國AACR年會分論壇做大會報告。兼職中國藥理學會化藥專業(yè)委員會,專業(yè)委員;中國老年學和老年醫(yī)學學會腫瘤分會,專業(yè)委員。擔任Nature communications等雜志審稿人. 曾任歐洲SCI雜志Contemporary Oncology副主編。實驗室目前有充足的經費,非常有前景的課題和成熟的實驗資源,誠聘具有生物學、免疫學、藥理學背景的博士后。
1.應聘者應具備的條件如下
(1)已獲得或即將獲得國內外知名大學的博士學位;
(2)有志從事科學研究,具有強烈的科研興趣,有意從事腫瘤免疫藥理學研究;
(3)具有積極向上的工作熱情,優(yōu)秀的學習能力,良好的學術道德和團隊合作精神。能獨立開展科研工作;
(4)獲得生物學或醫(yī)學領域博士學位,有分子生物學、細胞生物學和免疫相關研究經歷者優(yōu)先考慮;
(5)在國際主流學術期刊上發(fā)表過第一作者論文(IF大于5)。
2.崗位待遇:
(1)提供有競爭力的薪酬待遇,年薪20-30萬元左右;課題組優(yōu)先鼓勵申請人社部博新計劃、上海市超博、復旦大學超博等(具體參考: https://mp.weixin.qq.com/s/hurbGXoXfvPPpgkjLal4Ww),超級博士后年薪28-40萬;
(2)學校提供人才公寓,保障全職博士后的住房需求;
(3)博士后期間,發(fā)表高水平SCI論文可享受課題組獎勵政策;
(4)為全職博士后提供醫(yī)療保險、體檢服務等保障;
(5)充分發(fā)揮復旦大學優(yōu)質基礎教育資源,積極保障全職博士后子女入學;
(6)博后期間表現(xiàn)優(yōu)異者,可優(yōu)先機會留在復旦大學工作(有編制);
(7)特別優(yōu)秀者在待遇方面還可進一步商榷。
3.應聘材料遞送
請應聘者將個人簡歷(包括學習工作經歷、主要研究工作內容、發(fā)表論文、獎勵情況、個人近照等)、學歷學位證書復印件、1-2封推薦信及推薦人的聯(lián)系方式(可在初審通過后提供),發(fā)送至:zhudi@fudan.edu.cn。E-mail標題請注明"應聘博士后崗位+姓名"。對符合要求者將盡快安排面試。
應聘材料單位將予以保密。此招聘信息長期有效。
研究方向
1、靶向BCL9/β-catenin的藥理學機制研究。
2、腫瘤免疫治療新藥開發(fā)。
科研項目
1、2018,上海市科委科研計劃項目,“Wnt信號通路調控的腫瘤免疫微環(huán)境在結腸癌免疫抵抗的研究”,主持。
2、2018,上海市科委科研計劃項目,“結腸癌靶向EPCAM1通用型CART細胞治療研究”,參與。
3、2018,復旦大學自主研究課題融合基金,“Fzd4在腫瘤干細胞中的研究和新抑制劑開發(fā)”,主持。
4、2019,國家自然科學基金面上項目,“用于癌癥免疫治療新型RORγt激動劑的設計合成與作用機制研究”,參與。
5、2019,國家自然科學基金面上項目,“Wnt信號通路抑制劑調控腫瘤免疫微環(huán)境的機制研究”,主持。
6、2019,上海市科委生物醫(yī)藥領域科技支撐項目,“新型癌癥免疫治療藥物RORγt激動劑YWRQ-16的臨床前研究”,參與。
7、2019,復旦大學-中國科學院上海藥物研究所融合基金項目,“基于單細胞測序技術的肝癌細胞圖譜解析及新型生物標記物的發(fā)現(xiàn)和鑒定”,主持。
8、2019,復旦大學“卓越2025”人才培育計劃卓識計劃,主持。
9、2020,上海市科委“科技創(chuàng)新行動計劃”國際合作項目,“新型親環(huán)素抑制劑抗新型冠狀病毒的研究”,主持。
10、2021,復旦大學先導項目,結腸癌免疫治療關鍵技術研究,主持。
11、2021,國家自然科學基金面上項目,“BCL9/9L調節(jié)T細胞的腫瘤浸潤改善PD-1治療耐藥的研究”,主持。
代表性專利:
[1]靶向EpCAM抗原的CAR-NK細胞及其制備與應用, 2022-2-28, 中國, 202210187618.8。
[2]Zhu Di;Stabilized BCL9 Peptides for Treatment of Aberrant Wnt Signaling,2017/04/13,US,WO2017/062518 A1
[3]Zhu DI; Carrasco Ruben; Compositions and Methods for Treating Malignancies, 2016/04/7, US,WO2016/054354 A1
發(fā)明公開:
[1]樊嘉, 朱棣, 楊欣榮, 胡博, 吳隨一, 朱遠遠, 孫嘉磊, 周儉. 靶向BCL9/β-catenin復合體的先導肽[P]. 上海市: CN117801074A, 2024-04-02.
[2]趙玉軍, 朱棣, 周飛龍, 嚴子琴, 劉成龍, 曾子余, 程穎. 具有芐氧基芳基醚結構的化合物及其制備方法和用途[P]. 上海市: CN117177969A, 2023-12-05.
[3]趙玉軍, 朱棣, 周飛龍, 嚴子琴, 劉成龍, 曾子余, 程穎. 具有芐氧基芳基醚結構的化合物及其制備方法和用途[P]. 上海市: CN116768870A, 2023-09-19.
[4]李建其, 朱棣, 張慶偉, 劉成龍, 張浩, 沈櫟安, 王冠. β-catenin/BCL9蛋白蛋白相互作用的小分子抑制劑及其應用[P]. 上海市: CN116444420A, 2023-07-18.
[5]李建其, 朱棣, 張慶偉, 劉成龍, 張浩, 沈櫟安, 王冠. β-catenin/BCL9蛋白-蛋白相互作用的小分子抑制劑及其應用[P]. 上海市: CN116162056A, 2023-05-26.
[6]樊嘉, 徐泱, 朱棣, 胡博, 喻敏成, 孫嘉磊, 馬曉路, 吳隨一, 周儉. 一種癌癥免疫治療療效和預后預測試劑盒[P]. 上海市: CN115575620A, 2023-01-06.
[7]朱棣, 王永輝, 謝瓊, 田恩銘, 夏莉, 郁明誠. 一種RORγ激動劑及其在制備治療腫瘤疾病藥物以及促進Type17細胞分化中的應用[P]. 上海市: CN115521233A, 2022-12-27.
[8]朱棣, 余科, 吳重恩. 一種CAR-T治療載體及其構建方法和應用[P]. 上海市: CN115125272A, 2022-09-30.
[9]樊嘉, 徐泱, 朱棣, 胡博, 喻敏成, 孫嘉磊, 馬曉路, 吳隨一, 周儉. 抗PD-1抗體與IFN-α聯(lián)合在制備抗腫瘤藥物中的用途[P]. 上海市: CN114917335A, 2022-08-19.
[10]徐宇秋, 許劍民, 湯文濤, 呂洋, 吉美玲, 朱棣. 基于活化B細胞表達的結腸癌預后診斷用標記物及其用途[P]. 上海市: CN114019163A, 2022-02-08.
[11]徐宇秋, 許劍民, 湯文濤, 呂洋, 吉美玲, 朱棣. 基于B細胞表達的結腸癌預后診斷用標記物及其用途[P]. 上海市: CN113834941A, 2021-12-24.
[12]朱棣. EpCAM-CAR-T和hsBCL9-(CT)-24的組合物在制備抗腫瘤藥物中的應用[P]. 上海市: CN112516298A, 2021-03-19.
[13]朱棣, 陸偉, 陸路, 劉成龍, 魏國光, 徐巍, 夏帥. CsA脂質體在制備抗SARS-CoV-2藥物中的應用[P]. 上海市: CN112472791A, 2021-03-12.
[14]朱棣, 馮梅. 一種抗腫瘤的多肽及其應用[P]. 上海市: CN110003312A, 2019-07-12.
發(fā)明授權:
[1]朱棣, 王永輝, 謝瓊, 田恩銘, 夏莉, 郁明誠. 一種RORγ激動劑及其在制備治療腫瘤疾病藥物以及促進Type17細胞分化中的應用[P]. 上海市: CN115521233B, 2024-02-09.
[2]徐宇秋, 許劍民, 湯文濤, 呂洋, 吉美玲, 朱棣. 基于B細胞表達的結腸癌預后診斷用標記物及其用途[P]. 上海市: CN113834941B, 2024-01-05.
[3]朱棣. 一種靶向EpCAM-CART細胞與hsBCL9CT-24的組合在抗腫瘤中的應用[P]. 上海市: CN112516298B, 2022-11-01.
[4]趙玉軍, 朱棣, 周飛龍, 嚴子琴, 劉成龍, 張希晨. 一種具有芐氧基芳環(huán)結構的化合物,其制備方法和用途[P]. 上海市: CN112028870B, 2021-11-05.
代表性論著:
1.Hu, B., Yu, M., Ma, X., Sun, J., Liu, C., Wang, C., Wu, S., Fu, P., Yang, Z., He, Y., Zhu, Y., Huang, C., Yang, X., Shi, Y., Qiu, S., Sun, H., Zhu, A., Zhou, J., Xu, Y., Zhu, D.*, Fan, J.* Interferon-α potentiates anti-PD-1 efficacy by remodeling glucose metabolism in the hepatocellular carcinoma microenvironment. Cancer Discov., 2022. DOI: 10.1158/2159-8290.CD-21-1022 (IF: 39.4)
2.Xia, L., Tian, E., Yu, M., Liu, C., Shen, L., Huang, Y., Wu, Z., Tian, J., Yu, K., Wang, Y., Xie, D., Zhu, D.* RORγt agonist enhances anti-PD-1 therapy by promoting monocyte-derived dendritic cells through CXCL10 in cancers. J Exp Clin Canc Res. 2022. DOI : 10.1186/s13046-022-02289-2 (IF: 11.1)
3.Feng, M., Wu, Z., Zhou, Y., Wei, Z., Tian, E., Mei, S., Zhu, Y., Liu, C., He, F., Li, H., Xie, C., Jin, J., Dong, J., Yang, D., Yu, K., Qian, J., Lambrechts, D.*, Wang, M.*, Zhu, D.* BCL9 regulates CD226 and CD96 checkpoints in CD8+ T c ells to improve PD-1 response in cancer. Signal Transduct Target Ther, 2021, 6, 313. (5 year IF: 22.1)
4.Wang, X., Feng, M., Xiao, T., Guo, B., Liu, D., Liu, C., Pei, J., Liu, Q., Xiao, Y., Rosin-Arbesfeld, R., Shi, Y., Zhou, Y., Yang, M., Feng, Y., Jiang, Y., Shao, Z., Yu, K.*, Zhu, D.* BCL9/BCL9L promotes tumorigenicity through immune-dependent and independent mechanisms in triple negative breast cancer. Oncogene, 2021, 40: 2982- 2997. (IF: 9.8)
5.Liu, C., Zhou, F., Yan, Z., Shen, L., Zhang, X., He, F., Wang, H., Lu, X., Yu, K., Zhao, Y.*, Zhu, D.* Discovery of a novel, potent, and selective small-molecu le inhibitor of PD-1/PD-L1 interaction with robust in vivo anti-tumor efficacy. Br. J. Pharmacol., 2021, 178(13): 2651-2670. (IF: 8.7)
6.Tian, E., Yu, M., Feng, M., Wang, Y., Xie, Q.*, Zhu, D.* RORγt agonist synergizes with CTLA-4 antibody to inhibit tumor growth through inhibition of Treg cells via TGF-β signaling in cancer. Pharmacol.Res., 2021, 172:105793. (IF: 7. 6)
7.Feng, M., Zhao, Z., Yang, M., Ji, J., Zhu, D.*, T-cell-based immunotherapy in colorectal cancer. Cancer Lett., 2021, 498(40): 201-209. (IF., 8.6)
8.Yunbin Zhang; Jingjing Song; Zhongwei Zhao; Mengxuan Yang; Ming Chen; Chenglong Liu; Jiansong Ji; Di Zhu*. Single-cell transcriptome analysis reveals tumor immune microenvironment heterogenicity and granulocytes enrichment in colorectal cancer liver metastases, Cancer Letters, 2020, 470: 84-94.
9.Zhang Y, Zhang N, Chen M, Zhu D*. Targeting tumor immune microenvironment for cancer therapy in human gastrointestinal intestine malignancies. Cancer Letter. 458:123-135 (2019). DOI:10.1016/j.canlet.2019.05.017.
10.Feng, M., Jin, J., Xia, L., Xiao, T., Mei, S., Wang, X., Huang, X., Chen, J., Liu, M., Chen, C., Raf, S., Zhu, A., Feng, Y.*, Zhu, D.* Pharmacolo gical inhibition of β-catenin/BCL9 interaction overcomes resistance to immune checkpoint blockad es by modulating Treg cells. Science Advances., 2019, 5(5): 1-16. (IF: 14.1)DOI: 10.1126/sciadv. aau5240.
11.Zhu, D., Wang, Z., Zhao, J., Calimeri, T., Meng, J., Hideshima, T., Fulciniti, M., Kang, Y., Ficarro, S., Tai, Y., Hunter, Z., McMilin, D., Tong, H., Mitsiades, C., Wu, C., Treon, S., Dorfman, D., Pinkus, G., Munshi, N., Tassone, P., Marto, J., Anderson, K., Carrasco, R.* The Cyclophilin A–CD147 complex promotes the proliferation and homing of multiple myeloma cells. Nat Med., 2015, 21(6): 572-580. (IF: 53.4)
12.Takada, K.#, Zhu, D.#, Bird, GH. #, Sukhdeol, K., Zhao, J., Mani, M., Lemieux, M., Carrasco, D., Ryan, J., Horst, D., Fulciniti, M., Mushi, NC., Xu, W., Kung, AL., Shivdasani, R., Walensky, L.*, Carrasco, R.* Targeted Disruption of the BCL9/β-Catenin Complex Inhibits Oncogenic Wnt Signaling. Sci Transl Med., 2012, 4(148): 1-13. (IF: 17.9 )
獲得獎項
1、2024年 復旦大學優(yōu)秀博士學位論文指導導師。
2、2024年 第三十五屆上海市優(yōu)秀發(fā)明選拔賽優(yōu)秀發(fā)明銅獎。
3、2023年 中國抗癌協(xié)會科技獎二等獎。
4、2022年 上海生物工程學會“東富龍”生物工程優(yōu)秀青年科學家獎。
5、2019年 增愛·長木學術獎,增愛中國基金會。
6、2014 年,科技部教育部“春暉杯”創(chuàng)業(yè)大賽紐約賽區(qū)三等獎。
7、2013年,北美高層次人才創(chuàng)新大賽全美第六名。
8、2012年,創(chuàng)業(yè)世界杯波士頓地區(qū)第二名中國創(chuàng)新創(chuàng)業(yè)大賽全國百強。
9、2011年,MIT VS Harvard商業(yè)案例比賽決賽Finalist。
10、2010年,歐洲生物化學與分子生物學聯(lián)盟FEBS YTF Fellowship。
朱棣課題組

1. 課題組研究方向
課題組研究方向為靶向BCL9/β-catenin的藥理機制和腫瘤免疫新療法開發(fā)。具體方向為BCL9對免疫細胞的調控、BCL9對腫瘤微環(huán)境的調節(jié)以及促進免疫響應的新療法的開發(fā)。
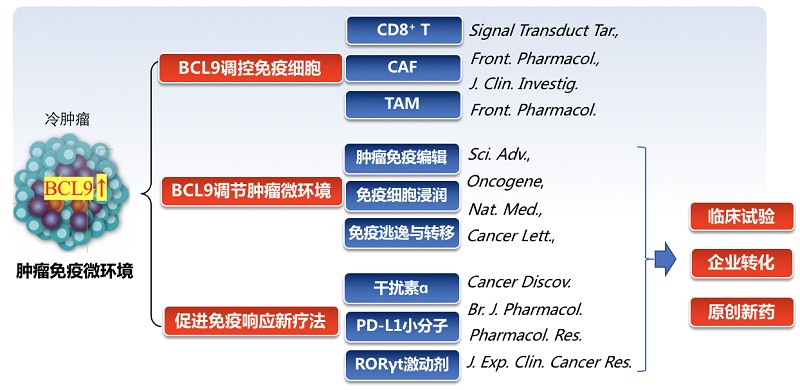
2. 課題組主要研究成果
代表性論文
代表性成果1:發(fā)現(xiàn)干擾素α增強肝癌PD-1抗體免疫療法的藥效并揭示藥理學作用機制
Hu, B et al. Cancer Discov 2022, DOI: .org/10.1158/2159-8290.CD-21-1022
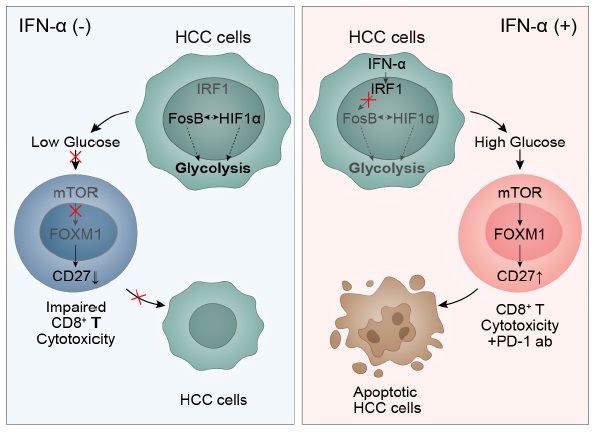
干擾素和抗PD-1抗體的組合導致了腫瘤微環(huán)境的重新編程,導致腫瘤中積累了高葡萄糖。這導致具有高代謝活性的 T 細胞亞型增加,可以更好地殺死腫瘤細胞。因為 T 細胞腫瘤殺傷活性的提高,這種聯(lián)合免疫療法治療將有更好的成功機會。
代表性成果2:發(fā)現(xiàn)BCL9改善癌癥中的PD-1反應的潛在機理
Feng, et al. Signal Transduct Target Ther. 2021;6(1):313.
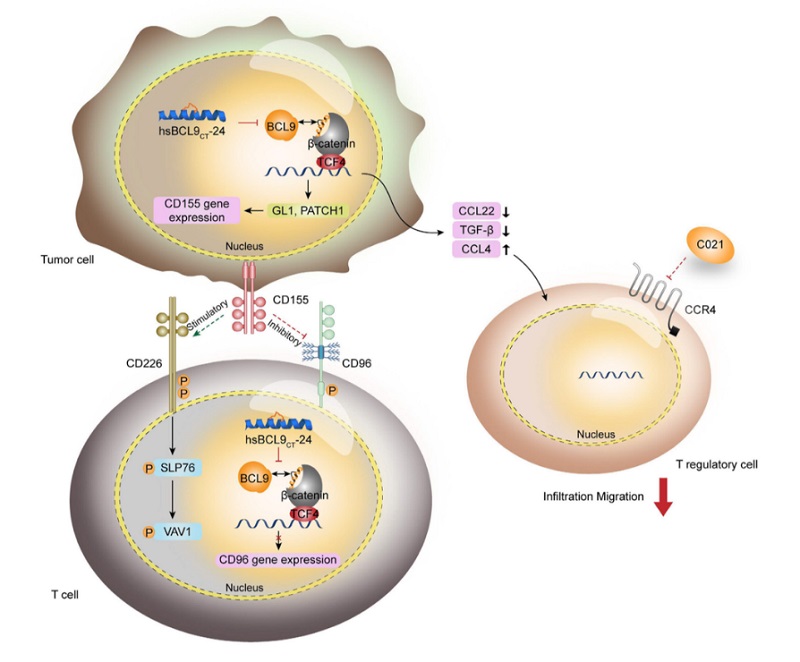
揭示了抑制BCL9能夠調節(jié)CD8+ T細胞的CD226和CD96免疫檢查點的平衡從而改善結腸癌患者對PD-1抗體的新分子機制。為結腸癌免疫治療新靶標提供理論基礎,為結腸癌免疫治療提供新的思路。
代表性成果3:發(fā)現(xiàn)靶向BCL9 /β-catenin促進 PD-1 抗體響應
Feng, et al. Signal Transduct Target Ther. 2021;6(1):313.
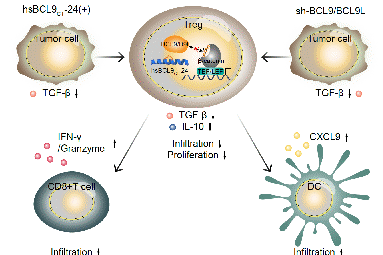
揭示了抑制BCL9能夠調節(jié)CD8+ T細胞的CD226和CD96免疫檢查點的平衡從而改善結腸癌患者對PD-1抗體的新分子機制。為結腸癌免疫治療新靶標提供理論基礎,為結腸癌免疫治療提供新的思路。
3.近年來獲批的重點項目或國家級人才項目
(1)國家自然科學基金面上項目,82073881,BCL9/9L調節(jié)T細胞的腫瘤浸潤改善PD-1治療耐藥的研究,2021-01至2024-12,55萬元,在研,主持。
(2)上海市科委科研國際合作項目,新型親環(huán)素抑制劑的抗COVID-19新藥開發(fā),2020-10至2023-09,在研,50萬,主持。
(3)國家自然科學基金面上項目,81872895,Wnt信號通路抑制劑調控腫瘤免疫微環(huán)境的機制研究,2019-01至2022-12,57萬元,在研,主持。
(4)上海市科委科研計劃項目,18ZR1403900,Wnt信號通路調控的腫瘤免疫微環(huán)境在結腸癌免疫抵抗的研究,2018-06至2021-05,20萬元,完結,主持。
(5)中組部國家青年特聘人才項目,藥理學,癌癥新靶點的發(fā)現(xiàn),2016-2019,完結,主持。
4.主要學術貢獻
對于晚期結腸癌患者而言,缺乏有效治療手段。免疫治療是癌癥治療的革命性療法,其中 PD-1抗體的治療響應依賴于T細胞的浸潤。90%的結直腸癌中存在Wnt/β-catenin通路的異常激活,并且和免疫抵抗的“冷腫瘤”相關。Wnt信號通路小分子抑制劑在腫瘤治療領域的研究前景十分廣闊,但是開發(fā)β-catenin抑制劑的其他挑戰(zhàn)。
BCL9/β-catenin是Wnt信號通路的創(chuàng)新靶點,主要學術貢獻包括:
(1)在成藥性靶點驗證方向,靶向BCL9和β-catenin的結合抑制癌癥特異性Wnt信號通路,具有良好的安全窗口,通過靶向BCL9與β-catenin的結合可以潛在解決Wnt通路抑制劑成藥性的挑戰(zhàn)(Sci Transl Med.,2012)。
(2)在改善免疫耐藥方向, 發(fā)現(xiàn)了靶向阻斷BCL9和β-catenin結合,在結腸癌腫瘤中降低Treg的腫瘤浸潤,改善腫瘤微環(huán)境中有利于免疫反應的發(fā)生,促進PD-1抗體響應(Sci Adv.,2019);進一步研究發(fā)現(xiàn)抑制BCL9能夠調控CD226和CD96在CD8+ T細胞中的平衡,增強腫瘤免疫反應(Signal Transduct Target Ther,2021)。
(3)在腫瘤免疫微環(huán)境調控方向,發(fā)現(xiàn)BCL9調控腫瘤免疫微環(huán)境的多種細胞因子,促進腫瘤細胞的歸巢,和促進免疫抑制性細胞的腫瘤浸潤(Nat Med.,2015;Oncogene, 2021)。
5.課題組成員及成果情況概況
課題組目前在讀博士研究生5名,碩士研究生4,聯(lián)合培養(yǎng)博士后1。

成果情況如下:
基于前期工作Nature Medicine和Science Translational Medicine為基礎,課題組近5年圍繞“靶向BCL9如何調控的腫瘤免疫微環(huán)境和如何促進腫瘤免疫響應”的科學問題,復旦大學通訊作者文章在國際著名期刊Cancer Discovery, Signal Transduction and Targeted Therapy,Science Advances, Oncogene, British Journal of Pharmacology, Pharmacological Research等,單篇最高影響因子39.4
申請專利10項,2項專利兩項完成授權,2項專利已在企業(yè)實現(xiàn)轉化;研究成果中其中開發(fā)的2個藥物分子進入臨床前實驗,2項研究成果進入非注冊臨床試驗階段。目前主持各類基金11項,獲得獎項2項。指導學生11名,已經完成畢業(yè)3名,獲得國家獎學金2項等其它8項獎項。
研究成果被Nature Reviews Clinical Oncology、Nature Reviews Cancer等國際專業(yè)學術媒體報道,同時被知名國內媒體如文匯報,新民網,科學網,澎湃新聞,學術經緯等專題報道。
6.國際合作情況
(1)在上海市科委科研國際合作項目中,與德國慕尼黑大學的Albrecht教授合作開展“新型親環(huán)素抑制劑的抗新冠新藥開發(fā)”,研究成果已發(fā)表。
(2)與Tel Aviv University大學Rina教授開展Wnt信號通路相關的免疫學研究合作,研究成果目前已發(fā)表在Oncogene和Frontiers in Pharmacology雜志。
7.科普短文
如何突破復雜腫瘤免疫微環(huán)境改變“冷腫瘤”成“熱腫瘤”?
每年結腸癌病人有180萬人,結腸癌是我國死亡率居于第四位的癌癥,缺乏有效靶向治療手段。80%以上的病人存在一個關鍵的信號通路—Wnt通路的突變,但是目前尚未有靶向Wnt通路的藥物上市。免疫治療是抗腫瘤革命性療法,僅15%結腸癌的病人有效,腫瘤免疫微環(huán)境介導免疫耐藥相關,缺乏有效治療手段。
腫瘤細胞通過激活MAPK、WNT等信號通路獲得免疫耐受。免疫微環(huán)境分子分型及免疫治療耐藥機制不斷有新的發(fā)現(xiàn),開發(fā)新型免疫細胞在腫瘤治療中的新技術不斷出現(xiàn)。 因此,研發(fā)出具有突破復雜腫瘤免疫微環(huán)境治療的結腸癌藥物,改善人民健康和提高患者生存率有著重要意義,同時對于突破國外藥物專利限制,解決關鍵時刻不被“卡脖子”,具有重要的作用。
8.實驗技術平臺
(1)Wnt抑制劑藥物篩選模型-用于篩選靶向BCL9/β-catenin抑制劑
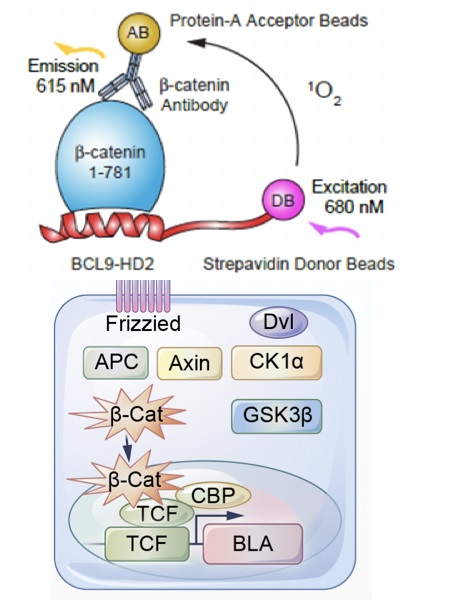
在穩(wěn)定表達LEF / TCF報告基因的HCT116細胞,檢測Wnt/β-catenin信號傳導的抑制效果。然后,選擇性細胞模型檢測細胞增殖及Wnt下游信號分子的影響,其中Colo320DM是β-catenin生長依賴型的結腸癌細胞系,RKO是非依賴型的結腸癌細胞。
(2)CFSE靶細胞殺傷篩選模型-用于篩選促進T細胞殺傷活力的分子
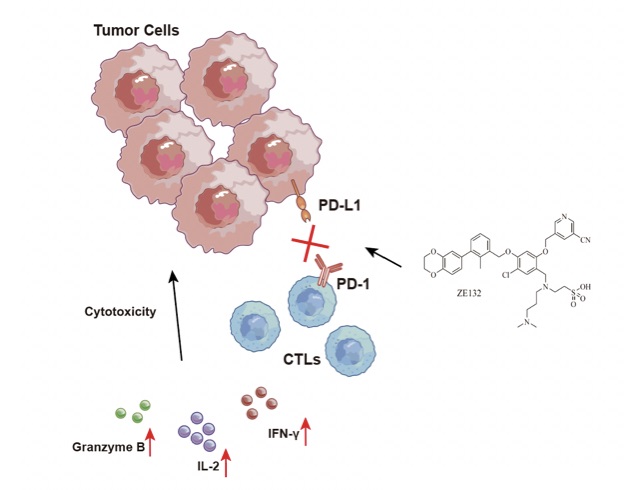
收集OT-I小鼠脾臟細胞,體外用OVA多肽刺激分化形成CD8+T細胞。用OVA多肽黏附靶細胞EL4,按照不同效/靶比將不同CD8+T細胞與CFSE標記的EL4細胞混合。將相等數(shù)量的CFSE標記的EL4細胞和EL4-OVA細胞混合均勻。效應細胞與靶細胞共培養(yǎng)。孵育后,流式上機檢測。
(3)Type17 細胞體外分化模型-用于篩選促進Type17分化的活性分子
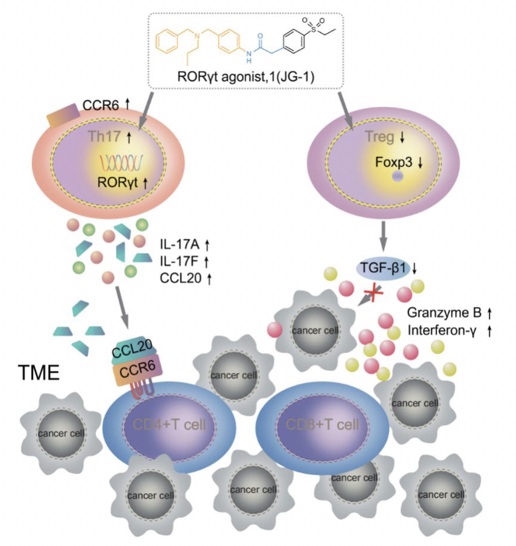
將Anti-CD3和Anti-CD28 進行48孔板包被。從小鼠中獲得淋巴細胞懸液。根據EasySep™ Mouse Naïve CD4+T Cell Isolation Kit,收集Naïve CD4+T細胞。利用細胞因子進行分化,Anti-IL-4, Anti-IFN-gamma,IL-6,TGF-β,培養(yǎng)體系重懸分選獲得的T細胞,每孔鋪入包被有CD3/CD28的48孔板中。